Alkadiēni: fizikālās īpašības, ķīmiskās īpašības un to pielietojums. Alkyddenu fizikālās īpašības: galds, fotoattēli, piemēri
Atkarībā no vairāku saišu skaita starpOglekļa atomos ir atdalītas vairākas ogļūdeņražu kategorijas. Sīki apskatīsim dienēnu savienojumus, to struktūras pazīmes, fizikālās un ķīmiskās īpašības.
Struktūra
Kas ir alkadiēni? Šīs organisko savienojumu grupas pārstāvju fiziskās īpašības ir līdzīgas kā alkānu un alkēnu īpašības. Dienes ar vispārīgo formulu CnH2n-2 ir sarežģītas saites, un tāpēc tās pieder pie nepiesātinātajiem ogļūdeņražiem.

Šīs saites var atrasties dažādās pozīcijās, veidojot dažādas dienes versijas:
- Kumulatīvi, kurā vairākas saites ir vienas oglekļa atoma divās sānās;
- konjugēts (konjugēts), kurā starp divām saitēm ir viens vienots;
- izolēts, kurā starp dubultajām saitēm ir vairākas atsevišķas sugas.
Šādās vielās ir visi ogļhidrātidubultsaite, ir sp2-hibrīda stāvoklī. Kādas ir alkadiēnu īpašības? Šādu savienojumu fiziskās īpašības nosaka tieši to struktūras īpatnības.
Nomenklatūra
Saskaņā ar sistemātisko nomenklatūru dienēogļūdeņražus sauc par tādu pašu principu, ko sauc par etilēna savienojumiem. Pastāv dažas atšķirīgas īpašības, kuras var viegli izskaidrot ar divu divu saišu klātbūtni molekulās.
Vispirms ir nepieciešams identificēt oglekļa skeletuGarākā oglekļa ķēde, kurā ir divas saites. Saskaņā ar oglekļa atomu skaitu, tiek izvēlēta bāzi nosaukumu, tad piedēklis-dien ir tam pievienots. Cipari norāda katras saites pozīciju, sākot ar mazāko.
Piemēram, saskaņā ar sistemātisko nomenklatūru pentadēn-1, 3 vielai ir šāda struktūra:
H2C = CH-CH = CH-CH3.
Sistemātiskajā nomenklatūrā ir daži izdzīvojušie vārdi: alēns, divinils, izoprēns.

Izomerizācijas veidi
Kardēdiāni, kuru fiziskās īpašības ir atkarīgas no oglekļa atomu skaita molekulā, ir vairāku veidu izomerisms:
- vairāku obligāciju pozīcijas;
- oglekļa skelets;
- starpklases tips.
Tagad pievērsīsimies jautājumiem par diēna ogļūdeņražu izomeru skaita noteikšanu.

Izomēru uzdevumi
"Noteikt izomēru savienojumu unNosauciet alkadiēnu fiziskās īpašības "- skolas mācību programmā organiskās ķīmijas stundās 10. klasē skolēniem tiek piedāvāti daudzi šāda veida jautājumi. Turklāt jūs varat izpildīt uzdevumus, kas saistīti ar nepiesātinātiem ogļūdeņražiem, vienā valstī eksāmenu ķīmijā.
Piemēram, visi sastāva C izomēri4H6, kā arī piešķir tiem nosaukumu sistemātiskajā nomenklatūrā. Pirmkārt, jūs varat veidot visus alkadiēnus, kuru fiziskās īpašības ir līdzīgas etilēna savienojumiem:
H2C = CH-CH = CH2.
Šis savienojums ir gāzveida viela, kas nešķīst ūdenī. Saskaņā ar sistemātisko nomenklatūru tam būs vārds butadiēna -1.3.
Ja vairākas saites tiek pārvietotas gar struktūru, ir iespējams iegūt izomēru šādā formā:
H3C-CH = CH = CH2
Tas ir šāds nosaukums: butadiēna -1,2
Papildus daudzkārtējās saites pozīcijas izomēriem, kompozīcijai C4H6 arī ir iespējams apsvērt starpklases izomerismu, proti, alkīniju klases pārstāvjus.

Diāna savienojumu sagatavošanas īpatnības
Kā iegūt alkadienus? Šīs klases pārstāvju fiziskās un ķīmiskās īpašības var pilnībā izpētīt tikai tad, ja ir racionālas metodes to laboratoriskajai un rūpnieciskajai ražošanai.
Ņemot vērā faktu, ka divinils un izoprēns ir vispopulārākais mūsdienu ražošanā, apsveriet iespēju iegūt dienē ogļūdeņraža datus.
Rūpniecībā šos nepiesātinātos savienojumus iegūst attiecīgo alkānu vai alkēnu dehidrogenēšanas procesā virs katalizatora, kas ir hroma oksīds (3).
Šā procesa izejvielas tiek izolētas saistītās gāzes vai naftas pārstrādes produktu pārstrādē.
Butadiēna-1,3 tika sintezēts no etanolaakadēmiķa Lebedeva dehidrēšanā un dehidratācijā. Kā pamatu divinilu rūpnieciskajai sintēzei tika izmantota šī metode, kas paredz, ka cinku vai alumīnija oksīdus izmanto kā katalizatoru un kas plūst 450 grādu temperatūrā. Šī procesa vienādojums ir šāds:
2 ° C2H5OH ------ H2C = CH-CH = CH2 + 2H2O + H2.
Turklāt mazu daudzumu var izolēt izoprēnu un divinilu, izmantojot eļļas pirolīzi.

Fizikālo īpašību īpatnības
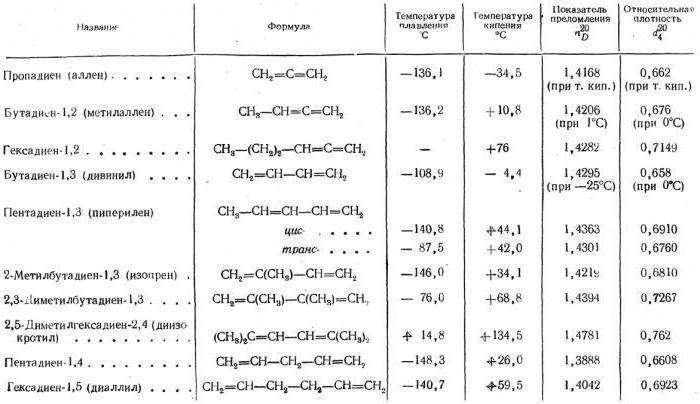
Kādā agregācijas stāvoklī ir alkadiens? Fizikālās īpašības, kuru tabulā ir informācija par kausēšanas un viršanas temperatūru, norāda, ka šīs klases apakšējie locekļi ir gāzveida stāvokļi ar zemu viršanas temperatūru un kušanas temperatūru.
Ar relatīvās molekulmasas palielinājumu pastāv tendence, ka šie rādītāji palielinās, pāreja no šķidruma agregācijas stāvokļa.
Tas palīdzēs jums detalizēti izpētīt alkadiena galda fiziskās īpašības. Attēli no produktiem, kas iegūti no šiem savienojumiem, ir minēti iepriekš.
Ķīmiskās īpašības
Ja mēs uzskatām, ka izolētas (nekonjugētas) dubultās saites, tām ir tādas pašas spējas kā tipiskajiem etilēna ogļūdeņražiem.
Mēs analizējām alkadienus fizikālās īpašības, to iespējamo ķīmisko mijiedarbību piemērus ņem vērā uz butadiēna -1,3.
Savienojumi ar konjugētām divpusējām saitēm ir augstākas reaktivitātes pakāpe salīdzinājumā ar citiem dieņu tipiem.

Savienošanās reakcijas
Visu veidu dienes raksturo reakcijas.savienojumi. Starp tiem mēs atzīmējam halogenēšanu. Šī reakcija noved pie dienēnas konversijas ar atbilstošo alkēnu. Ja ūdeņradis ir pārmērīgs, jūs varat iegūt piesātinātu ogļūdeņradi. Iedomājieties procesu kā vienādojumu:
H3C-CH = CH = CH2 + 2H2= N3C-CH2-CH2-CH3.
Halogenēšana ietver diāna savienojuma mijiedarbību ar hloru, joda, broma divatomu molekulu.
Hidrēšanas reakcija (ūdens molekulu pievienošana) unhidrohalogenēšana (attiecībā uz dienes savienojumiem, kuriem ir dubultā saite pirmajā pozīcijā) notiek saskaņā ar Markovņikova likumu. Tās būtība ir tāda, ka tad, kad saite ir salauzta, ūdeņraža atomi piesaista tiem oglekļa atomiem, kuriem ir mazāks daudzums ūdens gāzu, un hidroksilgrupas vai halogēna atomi pievienosies tiem C atomiem, kuros ir mazāks ūdeņraža daudzums.
Dienas sintēzes laikā diēnam pievieno etilēna savienojumu vai alkīna molekulu, kurai ir konjugētas dubultās saites.
Šo mijiedarbību izmanto dažādu organiskā tipa ciklisko savienojumu ražošanā.
Diāna pārstāvju polimerizācijasavienojumi ir īpaši svarīgi. Šajā procesā ir saistītas alkadiēnu fiziskās īpašības un to pielietojums. Polimerizācijas laikā tiek veidoti gumijas līdzīgi augsti molekulāri savienojumi. Piemēram, no butadiēna-1,3, butadiēna gumijas var iegūt, kam ir plašs rūpnieciskais pielietojums.
Atsevišķu dienna savienojumu raksturojums
Kādi alkadiēni satur fizikālās īpašības? Īsi analizējam izoprēna un divinila īpašības.
Butadiēna -1,3 ir gāzveida gāze,kam piemīt savdabīga smarža. Šis savienojums ir oriģinālie monomēri lateksa, sintētisko gumijas, plastmasas, kā arī daudzu organisko savienojumu ražošanai.
2-metilbuddīns-1,3 (izoprēns) ir bezkrāsains šķidrums, kas ir dabiskā kaučuka struktūras sastāvdaļa.
2-hlorbutadiēns-1,3 (hloroprēns) ir toksisks šķidrums, kas ir pamats vinila acetilēna ražošanai, sintētiskās hloroprēna gumijas rūpnieciskajai ražošanai.

Gumija un gumijas
Gumija un gumijas ir elastomēri. Visu kaučuku sadalījums ir sintētisks un dabisks.
Dabiskais kaučuks ir ļoti elastīgsmasa, kas iegūta no piena sulas. Latekss ir maza gumijas daļiņu suspensija ūdenī, kas pastāv tropu kokos, piemēram, Brazīlijas hevejā, kā arī dažos augos.
Šim nepiesātinātajam polimerim ir kompozīcija (C5H8) n, kuru vidējā molekulmasa svārstās no 15 000 līdz 500 000.
Pētījuma gaitā tika konstatēts, ka dabiskā kaučuka struktūrvienība ir formā -CH2-C = CH-CH2-.
Kā galvenais to atšķirtīpašības var atzīmēt lielisku elastību, spēju izturēt ievērojamas mehāniskās deformācijas, saglabāt formu pēc stiepšanās. Dažos ogļūdeņragos dabīgais kaučuks var izšķīst, veidojot viskoīdos šķīdumus.
Līdzīgi kā diēnu savienojumi, tas varpievienojiet pievienošanas reakcijas. Gutta percha ir izopēna polimēra veids. Šim savienojumam nav paaugstinātas elastības, jo tam ir atšķirības makromolekulu struktūrā.
Izgatavoti no gumijaszināmiem trūkumiem. Piemēram, ja temperatūra paaugstinās, tie kļūst lipīgi, maina to formu un, kad temperatūra pazeminās, tie kļūst pārāk trausli.
Lai atbrīvotos no šiem trūkumiem, rūpniecība izmantoja gumijas vulkanizāciju. Šī procesa būtība ir nodrošināt siltumizturību, elastību sēra apstrādē.
Process notiek temperatūras diapazonā140-180 ° C īpašās ierīcēs. Rezultātā veidojas gumija, kuras sēra saturs sasniedz 5%. Tā "šuj" gumijas makromolekulas, veidojot tīkla struktūru. Papildus sieram, gumijā ir arī papildu pildvielas: krāsvielas, plastifikatori, antioksidanti.
Pateicoties augstajam rūpnieciskajam pieprasījumam pēc gumijas izstrādājumiem, lielāko daļu no tā ražo sintētiski.





